Los aminoácidos no naturales se refieren a aminoácidos que no existen en animales y plantas, son raros en la naturaleza o se sintetizan artificialmente. Son derivados de aminoácidos naturales y se dividen principalmente en dos categorías. Una categoría son los análogos de aminoácidos con estructuras similares a las de los aminoácidos naturales, que se reflejan en la configuración opuesta, como D-alanina, D-fenilalanina, D-serina, etc. La otra categoría son los sustitutos de aminoácidos con estructuras que son bastante diferentes de los aminoácidos naturales.
Los aminoácidos no naturales tienen diversos grupos de cadenas laterales y propiedades estereoquímicas. Con el desarrollo y la promoción de la ciencia y la tecnología, se han utilizado ampliamente en muchos campos, como la medicina, la alimentación y la síntesis quiral. Los diversos grupos funcionales transportados por los AAU, como carbonilo, azida, alquinilo, alquenilo, amida, nitro, fosfato y sulfonato, permiten que las proteínas experimenten reacciones de modificación más complejas y diversas.
Los UAA tienen una gran especificidad y poco efecto sobre la estructura original de las proteínas, lo que los convierte en una poderosa herramienta para estudiar la estructura de las proteínas y su conformación dinámica. Por ejemplo, la introducción de aminoácidos fluorados en sitios clave de las proteínas puede observar eficazmente las señales de las proteínas en la resonancia magnética nuclear, simplificando así el proceso de recopilación y análisis de datos.
Además, la introducción de aminoácidos no naturales puede cambiar las propiedades físicas y químicas de las proteínas, como el pH y la estabilidad de la temperatura. En aplicaciones prácticas, se ha demostrado que los AAU mejoran eficazmente el rendimiento de las enzimas, incluido el aumento de la actividad y la estabilidad de las enzimas. Por ejemplo, reemplazar la tirosina natural número 309 de la fosfotriesterasa con L-(7-hidroxicumarin-4-il)etilglicina o L-(7-metilcumarin-4-il)etilglicina puede aumentar aún más la actividad catalítica de la enzima para la hidrólisis de paraoxon. entre 8 y 11 veces en función de su alta eficiencia original. Además, la incorporación de aminoácidos fluorados puede mejorar significativamente la estabilidad térmica de las enzimas. Por ejemplo, la parafluorofenilalanina fosfatasa puede seguir funcionando normalmente incluso a una temperatura elevada de 60 °C sin ningún impacto.
Los AAU tienen amplias perspectivas de aplicación en el campo de la biomedicina y también son los componentes principales de péptidos sintéticos y fármacos similares a péptidos en el país y en el extranjero.
Desde el descubrimiento de la penicilina, los antibióticos han salvado innumerables vidas y son aclamados como uno de los logros médicos más importantes del siglo XX. Sin embargo, el uso excesivo de antibióticos en la salud humana y animal ha generado la aparición de bacterias resistentes a los antibióticos, especialmente "superbacterias" multirresistentes, que han planteado una grave amenaza para la salud humana y animal.
Los péptidos antimicrobianos (AMP) son una clase de sustancias polipeptídicas básicas con actividad antimicrobiana. Han llamado la atención por sus características antimicrobianas de amplio espectro y su letalidad para ciertos patógenos resistentes a los medicamentos. Las diversas estructuras de los aminoácidos no naturales pueden cambiar significativamente la estructura y función de los AMP, como la hidrofobicidad, la densidad de carga y la actividad, después de reemplazar los aminoácidos naturales en los péptidos antimicrobianos. El grupo de investigación de Kang no sólo mejoró enormemente su actividad antimicrobiana contra las bacterias resistentes a la penicilina al reemplazar la lisina con ornitina en el péptido Cbf-14, sino que también redujo su citotoxicidad para las células de mamíferos. Vale la pena mencionar que los aminoácidos no naturales también pueden mejorar su eficacia antimicrobiana, selectividad celular y estabilidad de péptidos modificando los extremos C o N de los péptidos antimicrobianos. Por ejemplo, la modificación de la N-acetilación mejoró significativamente la eficacia antimicrobiana y la estabilidad de W-MreB.
Los aminoácidos no naturales no sólo tienen una amplia gama de aplicaciones en el campo de la biomedicina, sino que también exhiben excelentes propiedades catalíticas orgánicas. Actúan como catalizadores orgánicos, que generalmente no son tóxicos y son estables en comparación con otros métodos catalíticos, son insensibles a la humedad y al aire y muestran buena tolerancia a muchos grupos funcionales.
En el campo de la síntesis asimétrica, los aminoácidos α-no naturales pueden reemplazar eficazmente los catalizadores metálicos para lograr reacciones de síntesis asimétricas eficientes.
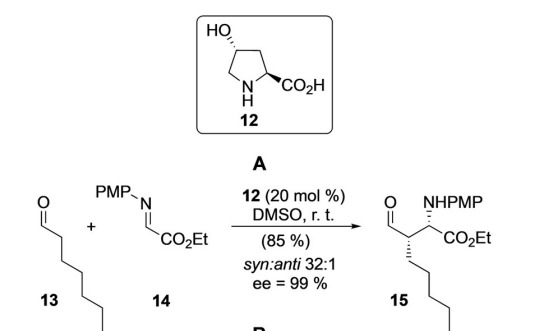
El equipo de Barbas utilizó (2S,4R)-4-hidroxiprolina como catalizador para catalizar con éxito la reacción de Mannich entre aldehídos grasos de cadena lineal e iminas, obteniendo bases de Mannich con excelentes rendimientos y estereoselectividad.
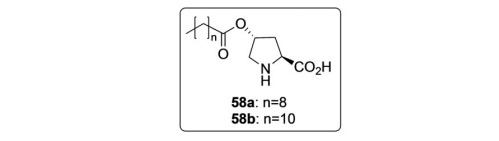
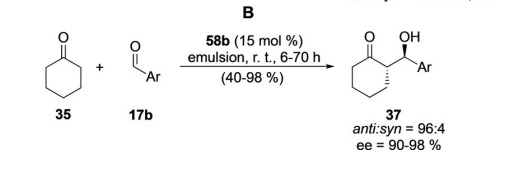
Además, el éster de trans-4-hidroxiprolina es anfifílico y es un tensioactivo. El equipo de Zhong utilizó esta propiedad para catalizar la reacción de condensación asimétrica de ciclohexanona y aldehídos aromáticos en un sistema de emulsión. Esta estrategia no sólo tiene una alta estereoselectividad, sino que también logra buenos rendimientos de reacción, lo que proporciona una nueva y poderosa herramienta para la síntesis asimétrica.
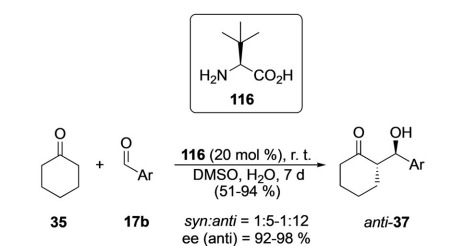
Otra clase de aminoácidos no naturales, la L-terc-leucina y sus derivados, también exhiben la capacidad de catalizar la síntesis asimétrica, catalizando eficazmente la reacción de condensación asimétrica de ciclohexanona y aldehídos aromáticos con buen rendimiento y estereoselectividad.
Los aminoácidos no naturales se utilizan ampliamente y son compuestos con valor importante y amplias perspectivas en muchos campos. Aunque su proceso de síntesis es bastante desafiante, con el avance continuo de la ciencia y la tecnología, seguramente se desarrollarán métodos de síntesis eficientes y ecológicos en el futuro, promoviendo así el desarrollo continuo del campo de los aminoácidos no naturales.
Haofan Bio ha estado profundamente involucrado en la investigación y el desarrollo de aminoácidos no naturales durante muchos años y actualmente cuenta con cientos de productos de aminoácidos no naturales. La siguiente tabla muestra algunos de los productos de aminoácidos no naturales. Los clientes con necesidades pueden llamarnos para realizar consultas.
Referencias:
[1] Zhao Mei, Liu Xinyuan, Qi Xianghui, et al. Avances de la investigación en síntesis de proteínas a partir de aminoácidos no naturales[J]. Industrias Alimentarias y de Fermentación. 2024, 8.
[2] Li Haining, Zhang Hongbing, Jia Zhenhua, et al. Aplicación y estrategia biosintética de aminoácidos no naturales[J]. Boletín de Biotecnología. 2023, 39, 43-55.
[3] Narancic, T.; Almahboub, SA; O'Connor, KE Aminoácidos no naturales: producción y potencial biotecnológico [J]. Mundo J Microbiol Biotechnol. 2019, 35, 67.
[4] Wang, XH; Yang, XM; Wang, QE; Meng, DM Aminoácidos no naturales: implicaciones prometedoras para el desarrollo de nuevos péptidos antimicrobianos [J]. Revisiones críticas en microbiología. 2023, 49, 231-255.
[5] Agirre, M.; Arrieta, A.; Arrastia, I.; et al. Organocatalizadores derivados de α-aminoácidos no naturales: alcance y aplicaciones [J]. Química. Asiático J. 2019, 14, 44-66.
[6] Zhong, L.; Gao, Q.; Li, C.; et al. Reacciones aldólicas asimétricas catalíticas directas sobre catalizadores quirales ensamblados en la interfaz de gotitas de emulsión [J]. J. Catal. 2007, 250.360-364.