I. Antecedentes Introducción:
Sin embargo, esta eficiente estrategia sintética cíclica de protección-condensación-desprotección aumenta significativamente el número de pasos de síntesis de péptidos, el consumo de reactivos y las operaciones engorrosas. Por lo tanto, la mejor solución es desarrollar un método que logre directamente reacciones de condensación cruzada de aminoácidos sin protección.
Recientemente, el equipo de Yamamoto, H. propuso una ruta sintética altamente eficiente y ecológica basada en reactivos de silicio: modificar aminoácidos con reactivos de silicio para hacerlos electrofílicos y nucleofílicos, y condensarlos directamente sin el uso de grupos protectores tradicionales para construir enlaces peptídicos eficientemente. Este método no solo simplifica los pasos sintéticos, sino que también demuestra una excelente practicidad.
II. Introducción del principio:
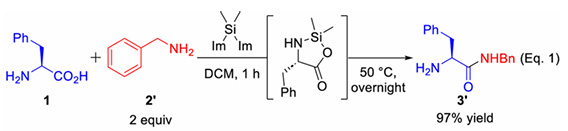
El núcleo de este estudio reside en el efecto sinérgico de dos tipos de reactivos de silano para lograr la formación de enlaces amida altamente selectivos entre aminoácidos no protegidos. Específicamente, una molécula de aminoácido reacciona con bis(1-imidazolil)dimetilsilano en diclorometano para producir un intermedio cíclico electrófilo de cinco miembros que contiene silicio, el cual puede actuar como donante de acilo para experimentar reacciones posteriores con otros nucleófilos y generar los productos correspondientes (véase la Figura 1); otra molécula de aminoácido forma un éster de aminoácido-TMS como nucleófilo bajo la acción combinada de N-trimetilsililimidazolio (TMS-IM) y N,O-bis(trimetilsilil)trifluoroacetamida (BSTFA).
Figura 1
En este sistema, el BSTFA actúa principalmente como reactivo de sililación, mientras que el TMS-IM desempeña una doble función: reacciona con los aminoácidos para mejorar su solubilidad en diclorometano; y facilita el proceso de sililación. El efecto sinérgico de estos dos agentes mejora significativamente la selectividad de la reacción, obteniendo un dipéptido cíclico de silano con la secuencia correcta mediante las reacciones electrofílicas y nucleófilas.
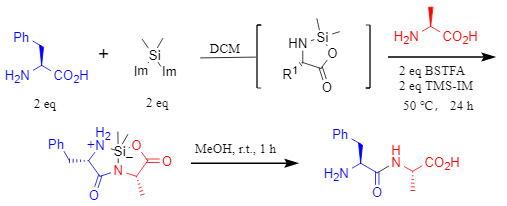
Además, el dipéptido cíclico de silano resultante presenta una buena estabilidad en condiciones normales, requiriendo únicamente un tratamiento rápido con metanol a temperatura ambiente para obtener el dipéptido sin protección, lo que facilita la extensión o purificación posterior (Figura 2).
Figura 2
III. Aplicaciones:
1. Amplia aplicabilidad de sustrato y excelente estereoselectividad.
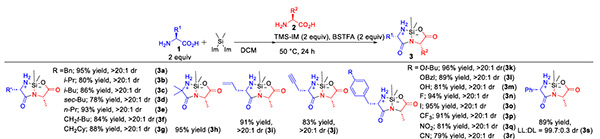
Esta estrategia sintética presenta buena compatibilidad con aminoácidos de diferentes estructuras (Figura 3). Ya se trate de un aminoácido con una cadena lateral estéricamente impedida o de un derivado de fenilalanina con diferentes propiedades electrónicas, el producto objetivo puede obtenerse con un alto rendimiento (la mayoría superior al 80 %), y la estereoconfiguración del aminoácido puede mantenerse correctamente (dr > 20:1). Incluso en el caso de la fenilglicina (Phg), propensa a la racemización, su estereoconfiguración puede mantenerse, lo que demuestra la superioridad de este método en términos de estereoselectividad.
Figura 3
2. Elongación eficiente de dipéptido a polipéptido
Los intermediarios dipeptídicos cíclicos de silano obtenidos mediante esta estrategia sintética son estables, fáciles de manipular y fácilmente convertibles en dipéptidos no protegidos, a la vez que proporcionan una plataforma única para la elongación de la cadena peptídica. Tanto el extremo N-terminal como el C-terminal pueden acoplarse directamente sin la participación de reactivos de condensación tradicionales para lograr la elongación de la cadena peptídica, evitando eficazmente la formación de oxazolona y los problemas de epimerización resultantes que se encuentran comúnmente en la síntesis de cadenas peptídicas largas.
Este estudio demuestra además el potencial de aplicación de esta estrategia en la construcción de secuencias complejas. A través de la condensación directa entre tripéptidos cíclicos de silano, se construyeron con éxito secuencias hexapeptídicas y heptapeptídicas (Figura 4), con la estructura principal heptapeptídica ampliamente encontrada en numerosas moléculas de fármacos como esmeglutida y telpósido. Esta estrategia sintética "convergente", que ensambla secuencias objetivo uniendo directamente segmentos peptídicos, simplifica significativamente el proceso sintético y proporciona un nuevo enfoque para la preparación de péptidos complejos y fármacos peptídicos.
Figura 4
IV. Conclusión general:
En resumen, este estudio desarrolló un método para la formación de enlaces peptídicos químicamente selectivos sin protección entre aminoácidos, basado en reactivos de silicio, y logró la síntesis de péptidos agregados. Este método no solo reduce significativamente el número de pasos sintéticos y el consumo de reactivos, sino que también proporciona una vía conveniente para la preparación de péptidos diana en condiciones suaves. Este avance proporciona una nueva vía sintética para el campo de la síntesis de péptidos y se espera que impulse el desarrollo de fármacos peptídicos y la investigación relacionada.
Introducción de la empresa:
Suzhou Highfine Biotech Co., Ltd. (Código bursátil: 301393.SZ), fundada en 2003 y con sede en la Zona de Alta Tecnología de Suzhou, es una empresa nacional de alta tecnología que proporciona materias primas especializadas a empresas globales de I+D y fabricación farmacéutica. Sus productos se utilizan principalmente en la síntesis de péptidos, nucleótidos y fármacos, abarcando una amplia gama que incluye agentes condensantes para la formación de enlaces amida especializados, agentes protectores, agentes de enlace, agentes de reticulación de proteínas para conjugados anticuerpo-fármaco, bloques de construcción moleculares, liposomas y reactivos de fósforo. Actualmente, ha desarrollado y producido más de 1500 productos.
A lo largo de más de dos décadas de incansable esfuerzo y acumulación, Highfine Biotech ha profundizado continuamente su experiencia en el campo global de reactivos para la síntesis de péptidos y se ha convertido en una empresa líder con una amplia gama de productos personalizados y ventajas significativas en la producción a gran escala, capaz de satisfacer las necesidades específicas de diversos clientes. Invitamos cordialmente a los clientes interesados en nuestros productos a contactarnos para obtener más información y analizar oportunidades de colaboración.
Referencias:
[1] Formación de enlaces peptídicos entre aminoácidos no protegidos: Síntesis convergente de oligopéptidos. DOI: https://doi.org/10.1021/jacs.4c08049