3/26/2026
Como participantes vitales en los procesos vitales, los péptidos siempre han sido un foco de investigación en el campo de la síntesis química debido a la necesidad de métodos de síntesis eficientes y precisos. Los métodos tradicionales de síntesis de péptidos suelen implicar la activación del grupo carboxilo, convirtiéndolo en un éster activo u otra sustancia reactiva, que luego se acopla con un grupo amino en otra molécula. Aunque este método es ampliamente utilizado, generalmente se limita a la síntesis C→N y es propenso a reacciones secundarias como la racemización cuando se trata de aminoácidos sensibles como la cisteína. Para superar este obstáculo, el equipo de J.-M. Campagne ha adoptado un enfoque diferente, desarrollando un novedoso método de síntesis de péptidos basado en una estrategia de "activación inversa", es decir, la activación del grupo amino.
Como participantes vitales en los procesos vitales, los péptidos siempre han sido un foco de investigación en el campo de la síntesis química debido a la necesidad de métodos de síntesis eficientes y precisos. Los métodos tradicionales de síntesis de péptidos suelen implicar la activación del grupo carboxilo, convirtiéndolo en un éster activo u otra sustancia reactiva, que luego se acopla con un grupo amino en otra molécula. Aunque este método es ampliamente utilizado, generalmente se limita a la síntesis C→N y es propenso a reacciones secundarias como la racemización cuando se trata de aminoácidos sensibles como la cisteína. Para superar este obstáculo, el equipo de J.-M. Campagne ha adoptado un enfoque diferente, desarrollando un novedoso método de síntesis de péptidos basado en una estrategia de "activación inversa", es decir, la activación del grupo amino.
I. Pensamiento inverso: de "ácidos carboxílicos activados" a "aminoácidos activados".
La base de los métodos tradicionales reside en la activación del grupo carboxilo, mientras que el equipo de J.-M. Campagne trasladó ingeniosamente el sitio de activación al grupo amino. Utilizaron N,N'-carbonildiimidazol (CDI), un compuesto económico y fácilmente disponible, en presencia de trietilamina para reaccionar con ésteres de α -aminoácidos, generando y aislando un intermedio estable de éster de aminoácido carboxílico de N-imidazolio (Figura 1). Este intermedio es equivalente a un "grupo amino activado" y puede almacenarse de forma estable durante varios meses.
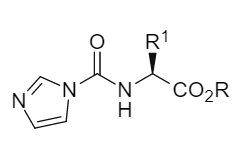
Figura 1. Fórmula general del éster de aminoácido N-imidazolílico.
En la síntesis de péptidos posterior, este intermedio reacciona directamente con aminoácidos N-protegidos en diclorometano en condiciones suaves, sin álcalis y en presencia de aditivos (HOBt/CuBr₂ ) , obteniéndose dipéptidos con un rendimiento del 52-90%. Este método es compatible con grupos protectores de carbamato de uso común, como Fmoc, Boc y Cbz, y no se observó racemización cuando el sustrato de reacción contenía cisteína fácilmente racémica. Sin embargo, los estudios indican que el disolvente convencional de síntesis de péptidos, DMF, no es adecuado para este sistema.
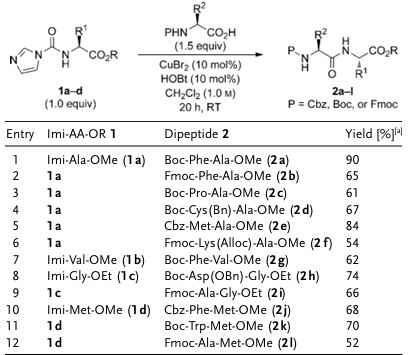
Figura 2. Síntesis de dipéptidos mediante "grupos amino activados”.
Para validar aún más el potencial de esta estrategia sintética, el equipo intentó sintetizar un tetrapéptido mediante la dirección N→C, obteniendo finalmente el producto deseado con un rendimiento del 25 % y sin encontrar productos racémicos. Este descubrimiento demuestra el gran potencial de este método para la síntesis inversa de péptidos, proporcionando una nueva ruta fiable para la síntesis de fármacos peptídicos complejos y moléculas bioactivas.
II. Síntesis en un solo paso: alta eficiencia, economía atómica y buena estereoselectividad.
Partiendo de trabajos previos, el equipo de J.-M. Campagne optimizó aún más la estrategia sintética y desarrolló un método de síntesis en un solo paso para dipéptidos. Este método, también llevado a cabo en condiciones suaves y neutras, no requiere álcali adicional y genera intermedios ésteres de aminoácidos carboxílicos de N-imidazolio in situ. Sin necesidad de separación ni purificación, estos intermedios pueden reaccionar directamente con aminoácidos protegidos disponibles comercialmente, lo que simplifica significativamente el proceso.
Los resultados experimentales demuestran que el método de síntesis en un solo paso permite obtener de forma eficiente diversos derivados de dipéptidos, con rendimientos de hasta el 87%, y es compatible con varios grupos protectores N-carbamato, exhibiendo una excelente estabilidad estereoquímica. Además, el estudio reveló que la prolina, debido a su estructura de amina secundaria, dificulta la síntesis de dipéptidos mediante activación amino.
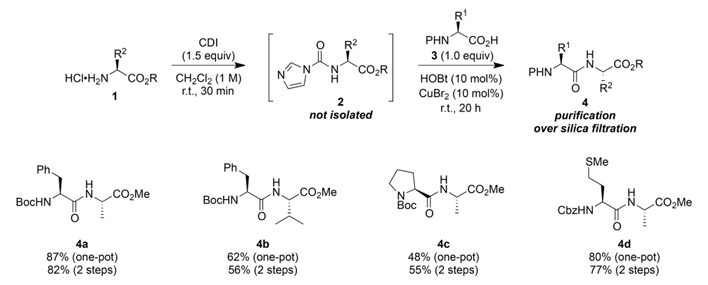
Figura 3. Síntesis en un solo paso de dipéptidos.
A diferencia del método de dos pasos, la estrategia de un solo recipiente utiliza el imidazol generado en el sistema como base durante la "activación del grupo amino", formando una sal de imidazol y eliminando así la necesidad de una base adicional. El estudio también reveló que añadir una base extra durante el proceso de acoplamiento dificulta la reacción de enlace amida entre el grupo amino activado y el ácido carboxílico.
III. Reacción asistida por microondas: acelera la reacción y acorta el tiempo de ciclo.
Para mejorar la eficiencia de la síntesis, el equipo de J.-M. Campagne introdujo además la tecnología asistida por microondas para explorar su aplicación en la estrategia de "activación de aminoácidos".
Basándose en la síntesis en dos etapas, se empleó irradiación por microondas para promover la reacción de enlace de las amidas (Figura 4). Los resultados mostraron que las microondas podían acelerar significativamente la velocidad de reacción, reduciendo el tiempo de reacción de 20 h en el método convencional a 1 h, manteniendo un buen rendimiento y sin observarse racemización. Además, se amplió la aplicación de este método a la síntesis de amidas convencionales, y el rendimiento cumplió con las expectativas.
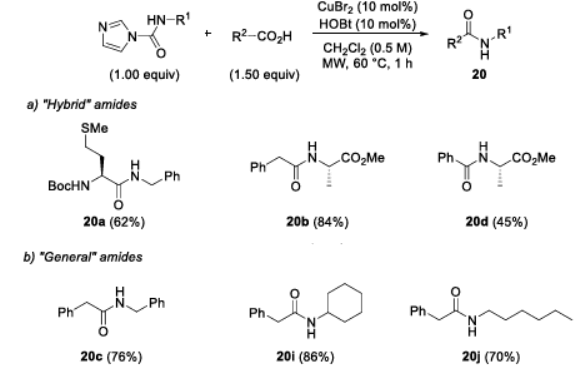
Figura 4. Síntesis de péptidos asistida por microondas.
Basándose en observaciones experimentales, el equipo propuso una posible ruta de reacción razonable (Figura 5): durante la reacción se forma un intermedio de anhídrido carbámico mixto , seguido de un reordenamiento intramolecular y la liberación de dióxido de carbono, generando finalmente el enlace peptídico deseado.
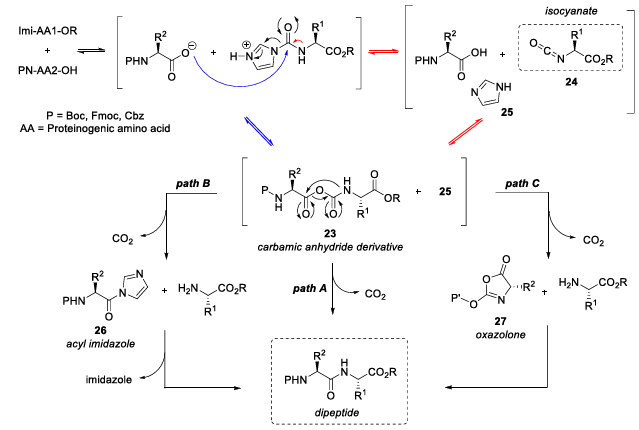
Figura 5. Mecanismo de reacción.
de α -aminoácidos mediada por CDI, desarrollada por el equipo de J.-M. Campagne, ofrece una nueva opción suave, práctica y con alta economía atómica para la formación de enlaces peptídicos. Este método no solo evita eficazmente el problema de racemización de aminoácidos sensibles durante la reacción, sino que también logra con éxito la compleja síntesis de péptidos en dirección N→C. Dado el creciente interés en el desarrollo de fármacos peptídicos, se espera que esta innovadora estrategia sintética se convierta en una herramienta fundamental para los investigadores.
Presentación de la empresa:
Suzhou Haofan Biotech Co., Ltd. (Código bursátil: 301393.SZ), fundada en 2003 y con sede en la Zona de Alta Tecnología de Suzhou, es una empresa nacional de alta tecnología que provee materias primas especializadas a empresas farmacéuticas de I+D y fabricación en todo el mundo. Sus productos se utilizan principalmente en la síntesis de péptidos, nucleótidos y productos farmacéuticos, abarcando una amplia gama que incluye agentes condensantes para enlaces amida especiales, agentes protectores, agentes de enlace, agentes de reticulación de proteínas para conjugados anticuerpo-fármaco, bloques de construcción moleculares, liposomas y reactivos de fósforo. Hasta la fecha, ha desarrollado y producido más de 1500 productos diferentes.
Tras más de dos décadas de esfuerzo constante y acumulación de experiencia, Haofan Biotech ha desarrollado continuamente su experiencia en el campo global de reactivos para la síntesis de péptidos. Actualmente, se ha consolidado como una empresa líder con una amplia gama de productos personalizados y ventajas significativas en la producción a gran escala, capaz de satisfacer las necesidades específicas de diversos clientes. Invitamos cordialmente a los clientes interesados en este producto a contactarnos para obtener más información y explorar oportunidades de colaboración .
Referencias:
[1] Síntesis inversa de péptidos mediante α-aminoésteres activados.
DOI: 10.1002/anie.201402147
[2] SecuencialEn una sola ollaSíntesisdeDipéptidosa través deelFormación transitoriadeProtegido por CDI-Nα-Aminoésteres .
DOI: 10.1002/adsc.201700034
[3] Activación de aminas: síntesis de dipéptidos "inversa” y formación de funciones amida a través de compuestos amino activados .
DOI: 10.1021/acs.joc.2c01288
Aquí compartimos nuestros productos relacionados más populares que pueden interesarle. Si tiene alguna pregunta, póngase en contacto con nosotros; nuestros especialistas le responderán en 24 horas.
Rellene el siguiente formulario y nuestro equipo de ventas estará encantado de ayudarle con un presupuesto sobre reactivos de síntesis peptídica.